
掃碼添加微信�����,獲取更多半導(dǎo)體相關(guān)資料
摘要
? ? ? 研究了氨過氧化氫溶液(SC-1溶液)���、Fe(III)����、Ni(Ii)����、Zn(II)在硅片上的吸附作用�����。實驗結(jié)果與平衡計算結(jié)果比較發(fā)現(xiàn)�,主要吸附物質(zhì)是溶解的中性氫氧化物配合物。計算出的氫氧化物配合物吸附的自由能變化支持了這一點�。
?
介紹
? ? ? 為了減少環(huán)境和設(shè)備的污染,開發(fā)和使用了多種清潔方案�。SC-1溶液(29%NH4OH:31%It202:H20=1:1:5體積比)1是半導(dǎo)體制造中廣泛使用的清潔溶液之一。然而�����,表面金屬污染是由溶液中的一些金屬雜質(zhì)引起的��。金屬雜質(zhì),特別是過渡金屬����,會引起電的惡化,例如柵極氧化物的分解����。
在本文中,我們通過平衡分析的方法研究了其吸附行為�。采用分析方法確定了吸附種類。同時還進(jìn)行了吸附的自由能計算��,以了解吸附的種類�,并支持平衡分析的結(jié)果。本文中檢測的金屬離子為Fe(III)����、Ni(II)和Zn(II)作為半導(dǎo)體制造中的典型污染物。
?
實驗
? ? ? 本工作中使用的以下化學(xué)物質(zhì)為EL級����,其中含有低于0.5ppb的過渡金屬雜質(zhì):50%HF、29%氫氧化銨��、31%H202、20%四甲基氫氧化銨�����。用于原子吸收分光光度法(AAS)的金屬標(biāo)準(zhǔn)溶液(1000ppm)用于故意污染��。本研究中使用的去離子水含有10ppt以下的過渡金屬雜質(zhì)����。所有的過程都在一個100級的潔凈室中進(jìn)行�����,濕化學(xué)品在房間的干凈通風(fēng)口中進(jìn)行處理�����。
?
結(jié)果和討論
? ? ? 圖2顯示了在SC-1溶液中獲得的Fe(III)�、Ni(II)和Zn(II)在硅晶片上的吸附等溫線。在大部分區(qū)域����,表面金屬濃度隨溶液中的濃度單調(diào)增加。對數(shù)對數(shù)線性表明���,本情況下金屬離子吸附受溶液與表面的化學(xué)平衡控制�。然而,表面Fe濃度在10~mol1-I以上表現(xiàn)出飽和趨勢��。這種吸附行為應(yīng)該與溶液中金屬離子的絡(luò)合態(tài)密切相關(guān)�����。
? ? ? 通過在SC-1溶液中加入一定量的四甲基氫氧化銨來控制pH�����,得到了Fe��、Ni�、~和Zn吸附的實驗pH依賴性。結(jié)果如圖所示11���,鐵和鎳對pH的依賴性明顯����,表明吸附種類為羥氧化物�����。然后將實驗中pH的依賴梯度與計算出的金屬氫氧化物在pH區(qū)10.5~12.0之間的金屬氫氧化物分布對pH的依賴梯度進(jìn)行了比較。如表二所示�,pH依賴性的實驗梯度與中性種Fe(III)和Ni(II)的計算值吻合較好。結(jié)果表明�����,吸附種類分別為Fe(OH)3(aq)和Ni(OH)2(aq)��。
另一方面��,本實驗中表面鋅的濃度與pH無關(guān)����,而計算出的氫氧化物配合物的分布具有明顯的pH依賴性。根據(jù)鐵和鎳的類比�,鋅的吸附種類也被認(rèn)為是中性氫酰胺復(fù)合物��。
?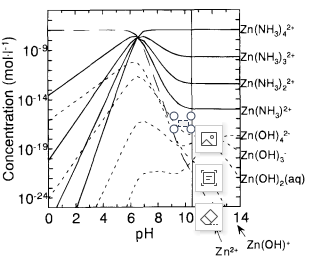
圖7 計算了鋅(ll)中氫氧化物和胺配合物的分布����。初始濃度應(yīng)為1x10-7molI-i??
總結(jié)
? ? ? 本文通過平衡分析和自由能計算,研究了Fe(III)���、NI(II(II)���、鋅(II)在硅片上的吸附作用���,得出了以下結(jié)論:
? ? ? 通過溶液中的平衡分析和TXRF角掃描測量,發(fā)現(xiàn)在SC-I溶液中��,鐵的固體中性氫氧化物Fe(OH)3(s)沒有吸附在硅片表面���。
固體Ni(OH)2和氫氧化鋅預(yù)計不會在SC-I溶液中形成��,因為可溶性胺配合物占優(yōu)勢�����。
? ? ? 自由能計算結(jié)果表明��,主要吸附物質(zhì)為溶解的中性羥氧化物�����。Fe(III)和NIi(II)的溶解中性氫氧化物配合物���,因為計算出的pH依賴分布的梯度與實驗吸附梯度很好地吻合。
??
文章全部詳情���,請加華林科納V了解:壹叁叁伍捌零陸肆叁叁叁